福建造!首款国产九价HPV疫苗获批上市背后的技术研发之路
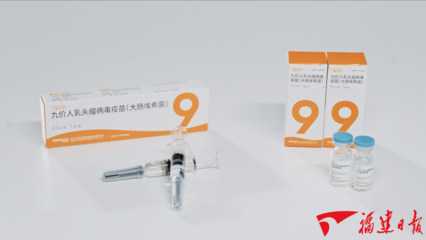
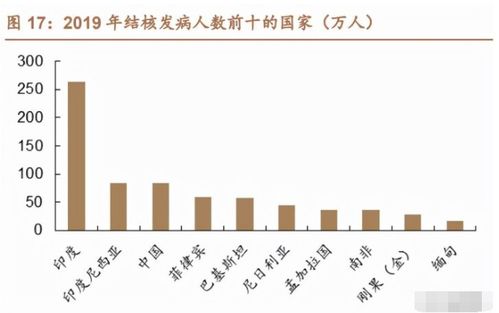
国家药品监督管理局正式批准由福建某生物制药企业研发生产的首款国产九价人乳头瘤病毒(HPV)疫苗上市。这不仅标志着我国在高端人用疫苗领域实现了重大突破,也意味着长期依赖进口、价格高昂的九价HPV疫苗市场格局即将被改写,将为我国适龄女性提供更可及、更普惠的预防选择。
这款疫苗的诞生,是生物技术研发领域一次系统性的攻坚成果。其核心技术研发路径,大体可分为几个关键阶段:
一、 抗原设计与表达系统的突破
九价HPV疫苗需要同时针对HPV 6、11、16、18、31、33、45、52、58型这九种高危和低危型别的病毒,制备出具有高度免疫原性的病毒样颗粒(VLPs)。研发团队首先在基因层面对这九种型别的L1衣壳蛋白基因进行优化设计,以提高其在表达系统中的产量和稳定性。选用了高效、安全的真核表达系统(如酵母或昆虫细胞-杆状病毒系统)进行规模化表达。这一环节的关键在于,必须确保表达出的VLPs在形态、结构上与天然病毒颗粒高度相似,从而能有效激发人体的免疫反应。
二、 复杂工艺的开发与放大
从实验室的“毫克级”样品到工业化生产的“千克级”产能,工艺开发是横亘在研发与上市之间的巨大鸿沟。这涉及到细胞大规模培养、病毒样颗粒的提取、纯化、组装等一系列复杂工序。研发团队需要建立稳定可控的发酵工艺、开发高效特异的层析纯化步骤以去除宿主细胞蛋白和DNA等杂质,并确保九种不同型别的VLPs能够按照既定比例高效、均一地组装。每一步的工艺参数都经过成千上万次的优化与验证,以确保最终产品的高纯度、高安全性和高有效性。
三、 严格的质量控制与评价体系
生物制品的质量控制贯穿研发始终。企业建立了远超国家标准的内控质量体系,运用高效液相色谱、毛细管电泳、电子显微镜、多种免疫学检测等先进分析技术,对疫苗原液和成品的理化性质、纯度、效力、安全性进行全方位、多维度的表征与放行检验。尤其是免疫原性评价,需要通过严谨的临床前及临床试验(I、II、III期),以科学数据证实其诱导产生的中和抗体滴度不劣于甚至优于进口同类产品,并能提供持久的保护。
四、 产能建设的同步推进
为了实现“福建造”乃至“中国造”的可靠供应,企业前瞻性地布局了符合国际GMP标准的大型现代化生产基地。从细胞库建立、发酵车间到纯化灌装线,全链条生产设施与研发进程紧密配合,确保了技术成果能够迅速转化为稳定、高质量的工业产品。
首款国产九价HPV疫苗的成功上市,是我国生物医药产业从“跟跑”到“并跑”乃至在部分领域“领跑”的生动缩影。它凝聚了我国科研人员与产业工作者十余年的心血,突破了跨国企业的技术壁垒与专利封锁。这不仅是一项产品的胜利,更是一套涵盖分子设计、工艺开发、质量管控、临床评价和产业化能力的完整生物制品研发技术体系的胜利。随着该疫苗的普及,有望大幅提升我国HPV疫苗接种率,为消除宫颈癌的公共卫生目标贡献关键力量,同时也将推动我国生物医药产业链的进一步升级与完善。
最新产品